 |
| 한미약품 '에모제졸' |
보건복지부는 한미약품의 역류성식도염치료제인 ‘에소메졸캡슐’이 6일(미국시간) 미국 식품의약국(FDA)로부터 국내 개발 개량신약 중 최초로 시판허가를 획득했다고 밝혔다.
미국을 포함한 북미 시장은 세계 의약품 시장의 약 37%(370조원 규모)를 차지한다.
그 동안 FDA으로부터 시판허가를 받은 제품은 국산 5호 신약(2002년12월27일 국내허가)인 팩티브(LG생명과학)와 인성장호르몬 밸트로핀(LG생명과학) 정도였다.
밸트로핀주(인성장호르몬)도 FDA 허가를 받았으나 시판은 하지 않았다.
에소메졸은 지난해 미국에서만 60억달러(IMS 기준)의 매출을 기록한 미국내 처방 1위 제품인 ‘넥시움정(아스트라제네카)’의 개량신약이다.
특히 이번 허가는 한미약품이 에소메졸의 미국 허가를 받기 위해 넥시움 개발사인 아스트라제네카와 2년여간 특허소송을 벌여 최근 에소메졸이 넥시움의 특허를 침해하지 않았다는 합의를 이끈 국내 최초의 사례다
FDA는 제네릭 등 업체가 시판허가를 신청할 경우, 이를 특허권자에게 통보하고 이에 대한 이의제기가 없을 경우에만 허가절차를 진행하고 특허침해 소송이 제기될 경우 최종허가를 유예한다. 오리지널 특허보유 제약사는 최장 30개월까지 제네릭 또는 개량신약의 제품 출시를 늦출 수 있다.
해치-왁스만 제도를 도입해 오리지널 제약사의 특허권을 FDA 허가와 연계한 운영으로 특허권자의 이익을 보호하기 위해서다.
따라서 한미약품은 넥시움 특허가 만료돼 제네릭이 출시되는 내년 5월까지 단독으로 시장을 공략하는 기회를 확보하게 됐다.
한미약품은 곧 미국 현지에서 제품명 '에소메프라졸 스트론티움'으로 미국 파트너사인 암닐을 통해 에소메졸을 출시할 계획이다.
복지부는 에소메졸 출시는 특허 도전을 통해 미국과 같은 선진국 시장에 진출하는 좋은 성공 모델이 될 수 있다는 점에서 국내 기업에 시사하는 바가 크다고 설명했다.
이와 함께 최근 미국의 의료보장 확대 정책에 따라 가격과 품질 경쟁력을 앞세워 세계 최대 시장인 미국에서 상업적으로 성공하는 최초의 국산 의약품이 될 가능성이 높다고 전망했다.
또한 정부가 제약시장 중 가장 큰 시장인 북미시장 진출을 위해 민·관 합동으로 추진했던 ‘콜럼버스 프로젝트’를 통해 미국 진출의 교두보를 마련했다는 점에서 의의가 있다고 밝혔다.
유럽의약품청(EMA) 바이오시밀러 허가, JW중외제약과 박스터간 3-챔버 영양수액제 수출계약, 보령제약 국산 신약 카나브정의 중남미 수출계약 체결 등 국내 기업의 다양한 글로벌 진출 사례가 증가하면서 올해는 제약산업 성장의 원년이 될 것으로 기대된다.
복지부 관계자는 "한미약품 에소메졸 외에도 LG생명과학·동아제약 등 상당수 제품이 미국에서 임상이 완료돼 올해안에 품목 허가가 가시화 될 것"이라고 말했다.
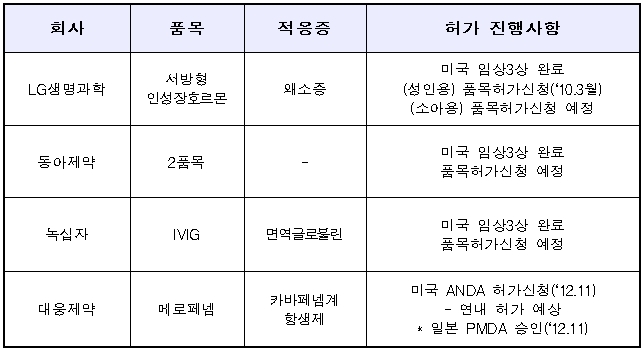 |
| <표> FDA 품목허가신청 품목 |
©'5개국어 글로벌 경제신문' 아주경제. 무단전재·재배포 금지


![[르포] 중력 6배에 짓눌려 기절 직전…전투기 조종사 비행환경 적응훈련(영상)](https://image.ajunews.com/content/image/2024/02/29/20240229181518601151_258_161.jpg)



